仕事で役立つ人気ビジネスアプリおすすめ!
[PR]
[PR]上記の広告は3ヶ月以上新規記事投稿のないブログに表示されています。新しい記事を書く事で広告が消えます。
東大など、コレラ毒素が細胞内に侵入する経路を発見
東京大学と科学技術振興機構(JST)は9月13日、コレラ菌が放出し、コレラを発症する原因となる「コレラ毒素」が細胞内に運ばれる経路を見出し、その運搬経路が毒素感染に必須であることを明らかにしたと共同で発表した。東京大学学院薬学系研究科の田口友彦特任准教授と新井洋由教授らが、JST課題達成型基礎研究の一環として行っている研究の成果によるもので、その成果は米国科学アカデミー紀要「Proceedings of the National Academy of Sciences of the United States of America」のオンライン速報版で9月12日の週(米国東部時間)に公開予定。
コレラは、コレラ菌(Vibrio cholerae)を病原体とし、激しい水様性の下痢を伴う致死的な経口細菌性感染症だ。小腸に到達したコレラ菌が放出するコレラ毒素によって、腸の表面にある細胞の機能が損なわれることによって発症する。コレラの感染力は大変強く、過去に幾度も世界的大流行を引き起こし、現在もコンゴ、ハイチなどではコレラ感染によって多くの人が死亡している。
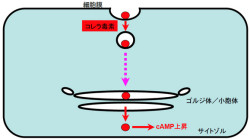
コレラ毒素は1つのAサブユニットと、5つのBサブユニットから構成されるタンパク質性の毒素で、AサブユニットがADP-リボシル化能を持つ酵素。コレラ毒素は腸表面の上皮細胞に取り込まれ、細胞小器官のゴルジ体や小胞体を通過しながら、最終的にサイトゾル(細胞質から細胞内小器官を除いた部分のこと)へ運搬され、次いで3量体Gタンパク質のADP-リボシル化を行うことで、3量体Gタンパク質の恒常的な活性化を引き起こす。その結果として「環状アデノシン一リン酸」(cAMP:cyclic adenosine monophosphate)の濃度が異常に上昇し、細胞、組織から電解質と水が大量に漏出することで、コレラ特有の激しい下痢が起きると考えられている。しかし、どのような細胞膜からゴルジ体へと運搬されるのかが不明だった(画像1)。
画像1。コレラ毒素の細胞内侵入経路。コレラ菌によって放出されたコレラ毒素(赤丸)は、小腸上皮細胞膜に発現している「GM1糖皮質」に結合し、細胞内へ取り込まれる。取り込まれた後は、ゴルジ体や小胞体を経由して最終的にサイトゾル(青色の部分)へ脱出し、cAMP濃度の上昇を引き起こす。ただし、細胞膜からゴルジ体へ至る輸送経路についてこれまでは不明だった
研究グループでは、アフリカミドリザルの細胞「COS-1細胞」が秩序だった細胞小器官の分布を持つという田口特任准教授らの2007年の発見を利用することで(画像2)、コレラ毒素の細胞内運搬経路を明らかにし、その運搬経路を制御する分子の同定を行う研究を行った。
画像2。COS-1細胞における細胞小器官の空間分布。COS-1細胞では、ゴルジ体はリング状の構造を取っており、その内側にリサイクリングエンドソームが存在する。この特徴がリサイクリングエンドソームの顕微鏡による観察を容易にした。ほかの細胞小器官はゴルジ体のリング構造の外側に分布する
今回明らかになったのは4点。1点目は、コレラ毒素は細胞膜から取り込まれた後、細胞膜へ再回収(リサイクル)する経路に関わる細胞小器官「リサイクリングエンドソーム」を経由してゴルジ体へ運ばれるということ(画像3)。
画像3。細胞に侵入した後のコレラ毒素の移動経路の可視化。蛍光標識したコレラ毒素をCOS-1細胞に取り込ませ、取り込ませた時間を0分として一定時間が経過するごとに観察を実施した。ゴルジ体は緑色で、コレラ毒素は赤で染色している。コレラ毒素が15分後にリサイクリングエンドソーム(ゴルジ体の形作るリング構造の内側)に運ばれ、75分後になってゴルジ体へ運搬されるのが容易に見て取ることが可能
細胞が細胞外の物質を取り込む営みを「エンドサイトーシス」と呼び、この営みによって取り込まれた物質が運ばれる細胞小器官を総称して「エンドソーム」と呼ぶ。リサイクリングエンドソームもエンドソームの一種であり、エンドサイトーシスで取り込まれた物質が細胞膜へ再回収する過程(リサイクル)で通過するエンドソームのことだ。
そして2点目は、リサイクリングエンドソームに局在する「エベクチン2タンパク質」が、コレラ毒素のリサイクリングエンドソームからゴルジ体への運搬を制御している点(画像4)。エベクチン2は生体内のほとんどの臓器や組織に存在しており、細胞内ではゴルジ体近縁部に存在している。ただし、その機能についてはこれまで未解析だった。
画像4。エベクチン2タンパク質欠失によるコレラ毒素の輸送遅延。Aはコレラ毒素を取り込ませてから一定時間後の様子を蛍光顕微鏡で観察した様子。左が通常細胞で、右がエベクチン2タンパク質欠失細胞。エベクチン2タンパク質欠失細胞では、15分後の時点で両細胞ともリサイクリングエンドソームまでコレラ毒素は集まっている。しかし、90分後に通常細胞は毒素がゴルジ体にまで到達しているが、欠失細胞ではまだリサイクリングエンドソームに留まっていることがわかる。Bはエベクチン2タンパク質欠失細胞では、cAMP濃度の上昇が、通常細胞(コレラ毒素添加あり)よりも抑えられているのがわかる
続いて3点目は、リサイクリングエンドソームには、リン脂質の一種である「ホスファチジルセリン」が豊富に存在するということ(画像5)。
画像5。リサイクリングエンドソーム中のホスファチジルセリンの可視化。ホスファチジルセリン(PS)と特異的に結合するタンパク質「LactC2」に蛍光タンパク質(GFP)をつなげたもの(画像中:PS結合タンパク質)をCOS-1細胞で発現させた。ゴルジ体体は赤色で、PS結合タンパク質は緑で染色。LactC2タンパク質がゴルジ体の内側(リサイクリングエンドソーム)に集積していることが見られることから、ホスファチジルセリンがリサイクリングエンドソームに豊富にあることが判明した
最後の4点目は、ホスファチジルセリンと結合するタンパク質「LactC2」を細胞内で過剰発現することによって、コレラ毒素のゴルジ体への輸送が抑制されることだ(画像6)。
画像6。ホスファチジルセリン(PS)に結合するタンパク質の過剰発現によるコレラ毒素の輸送遅延。ホスファチジルセリンに特異的に結合するLactC2タンパク質をCOS-1細胞で過剰に発現させて、その後、コレラ毒素の取り込みを行った。図には、2つの細部があり、矢印で示しているのがLactC2タンパク質を発現している細胞。*で示しているのが通常細胞だ。通常細胞では、コレラ毒素がゴルジ体に特着しているが、LactC2タンパク質を過剰に発現している細胞では、ゴルジ体に到達できずリサイクリングエンドソームで蓄積してしまっていることがわかる。つまり、LactC2タンパク質が過剰に存在するためにエベクチン2タンパク質がホスファチジルセリンと結合できなくなり、コレラ毒素が運ばれなくなったという
今回の研究によって、リサイクリングエンドソームの細胞内物質輸送における新しい機能「リサイクリングエンドソームからゴルジ体への輸送」と、リサイクリングエンドソームの重要な構成因子であるエベクチン2タンパク質とホスファチジルセリンが明らかとなった。
リサイクリングエンドソームから細胞膜への物質輸送は既に知られているが、ゴルジ体への物質輸送は今回初めて発見された機能である。これにより、赤痢菌が放出する「シガ毒素」や毒素原性大腸菌が放出する「易熱性エンテロトキシン」、ヒマの種子から単離される「リシン」など、サイトゾルへ輸送されることで毒性を発揮するほかの毒性タンパク質もリサイクリングエンドソームを介する輸送経路によってサイトゾルへ運ばれ、細胞毒性を発揮している可能性も出てきたという。
また今回の発見により、コレラ毒素のサイトゾルへの侵入をリサイクリングエンドソームの段階で阻害する薬剤開発を行うことが可能となった。さらに、毒素の持つ酵素活性を阻害する薬剤の開発だけではなく、物資輸送の視点に立脚した抗毒素薬の開発という新しい治療戦略が提唱された形だ。
そのほかに、リサイクリングエンドソームからゴルジ体への物資輸送経路が、毒素のためだけに細胞に備わっているとは考えにくいことから、細胞が通常時にこの運搬経路を使って輸送しているタンパク質を同定することで、リサイクリングエンドソームの新たな細胞生物学的機能を明らかにできる可能性も出てきたとしている。
IMS、広い波長領域での光吸収を可能にした二次元高分子を開発

自然科学研究機構 分子科学研究所(IMS)は、18π電子を有する大環状ポルフィリンやフタロシアニンからなる二次元高分子を合成したことを発表した。同二次元高分子は、紫外から近赤外まで幅広い波長領域での光吸収を可能にし、さらに、高い光伝導性を誘起できることから、新しい構成を有する太陽電池の構築などにつながる可能性があるという。
二次元高分子は、規則正しいポア構造を有する共有結合性高分子で、積層することで一次元チャネル構造を形成する。原理的に分子一層が一枚の原子シートを提供することができ、軽い元素を共有結合で連結して分子骨格を成し遂げているため、軽くて丈夫という特徴がある。また、ポアサイズは一義的に分子構造によって決定され、分子設計により思い通りの細孔を作ることができるため、設計可能な新しい多孔性物質として期待されている。
同研究所の江グループは、二次元高分子にπ電子系を導入することで、新しいπ電子系二次元高分子の合成を行っており、π電子系分子としてトリフェニレンやピレン、アントラセンなどの共役炭化水素化合物を用いてきたが、光エネルギー利用の観点からは、これらの分子は光吸収波長が紫外部に限定されてしまい、幅広い波長領域の光を吸収可能な分子構造が必要不可欠であった。
そこで同研究グループは、新たに18π電子を有する大環状ポルフィリンやフタロシアニンからなる二次元高分子を合成。ポルフィリンとその類似体は代表的な色素分子で、生体内では酸素運搬・貯蔵タンパクであるヘモグロビンやミオグロビンをはじめ、チチトクロームP-450酵素、植物やバクテリアにおける光捕集アンテナ系や光合成などの活性中心を担っている。一方、フタロシアニンは伝統的な顔料であり、近赤外領域に大きな吸収極大を持っており、研究グループでは、これらの大環状π分子を共有結合で二次元高分子骨格に織り込み、紫外から近赤外まで幅広い波長領域での光吸収を可能にし、さらに、高い光伝導性を誘起できることを確認した。
ポルフィリンとフタロシアニンの構造
ポルフィリンからなる二次元高分子は、反応時間を調整することでサイズをコントロールして任意のキューブ状構造を作ることができる。同キューブは、サイズが大きくなるにつれて、表面積やポア容積が次第に大きくなる。これは、高分子の高次構造を制御することができることを意味し、二次元高分子の精密合成という新しい局面を開くものだと研究グループでは説明している。
ポルフィリンからなる二次元高分子および積層によって形成された共有結合性有機骨格構造。 図中、青はポルフィリン環の炭素原子、白は水素原子、黄色は窒素原子、緑色は亜鉛などの金属原子を示す
一方、モノマーとしてフタロシアニンを用い、縮合反応により二次元高分子を合成した。フタロシアニンは互いに真上に来るようにスタックしているため、構造内ではあらかじめフタロシアニンからなるキャリア移動路が形成されている。実際、フタロシアニン二次元高分子は、1.6cm2V-1S-1という高いキャリア移動度を示したほか、二次元分子骨格はホール伝導であることが確認された。フタロシアニンからなる二次元高分子は紫外から近赤外まで幅広い光を効率よく捕集でき、光を照射すると、大きな光電流が誘起され、高い光伝導性を有することも判明した。
フタロシアニンからなる二次元高分子および積層構造。図中、水色はフタロシアニンの炭素原子、紫色は窒素原子、白は水素原子、緑色ニッケルなどの金属原子を示す
さらに研究グループでは、電子を流せるn型有機物は種類が限られた上、安定性において大きな問題が抱えていることの解決を目指し、二次元骨格のエッジ部位に電子吸引性分子を導入することで、新規n型二次元高分子の合成を行った。同二次元高分子は熱的に安定で、400℃でも分解することなく構造を保つことができる。πスタックによりカラム構造が形成され、高い電子移動度(0.6cm2V-1S-1)を示したという。また、光を照射したところ、速やかに光電流が誘起され、高い光伝導能を示した。これは、n型二次元高分子としては初めての例だという。
n型二次元高分子及び積層構造。図中、水色はフタロシアニンの炭素原子、紫色はベンゼン環、青色は窒素原子、黄色はイオウ原子、緑色はニッケルなどの金属原子を示す
なお、同二次元高分子は、幅広い波長領域を吸収することが可能で、高いキャリア移動度を兼備するため、光エネルギー変換、特に、太陽電池の新しい材料として期待できるという。特に、πスタックによって形成された積層構造を電極基板上に転写することができれば、新しい構成を有する太陽電池の構築が可能となり、効率的な光エネルギー変換システムの実現に繋がることが期待できると研究グループでは説明している。
NEDO、耳の軟骨から鼻の骨を再生させる技術を開発

新エネルギー・産業技術総合開発機構(NEDO)は、三次元複合臓器構造体研究開発の成果として、患者の耳からわずかな軟骨を取って、鼻の形の軟骨を再生させる技術(インプラント型再生軟骨)を開発、再生軟骨を口唇口蓋裂の患者の鼻に用いる臨床研究が東京大学で開始したことを発表した。
軟骨は鼻や耳の形を保ったり、関節のなめらかな運動を維持したりするための組織だが、先天性の異常や老化に伴う病気で一旦、欠損や変形ができてしまうと自然には治らず、顔の形が保てない、生活や仕事での動作ができない、などといった不自由が生じる。日本では、口唇口蓋裂の鼻の変形や小耳症、変形性関節症などを合わせると2000万人以上の人が、軟骨の何らかの病気にかかっているといわれている。
再生医療は、患者の身体の細胞や組織の一部を取って試験管の中で培養し、必要な組織や臓器を再生させて治療に使う医療で、自己修復する力に乏しい軟骨に対しては、体外で培養して人工的に軟骨をつくる再生医療の導入が期待されている。現在、液状あるいはゲル状の再生軟骨が使用可能になっている、硬さがないため顔面の高度な変形には直接使用できないのが現状であり、鼻や耳の形をした、十分な硬さと弾力性を持つ再生軟骨の開発が待たれていた。
これまで、顔面の軟骨の変形や欠損を治療するためには、身体の他の部位の軟骨や骨を移植する方法は行われてきたが、鼻の高度な変形を治すような大きな軟骨を採取することはできなかった。今回開発された技術は耳の目立たない部から採取されるわずかな軟骨を使用して、再生させるもので、耳の変形、気管の軟骨の欠損、そして将来は関節の軟骨の再建などに応用できるものと期待されるという。
具体的には、鼻に適した硬さと形を持った再生軟骨を開発した。作製方法は、まず、患者の耳の裏から5~10mm程度の少量の軟骨を採取して軟骨細胞を取り出す。この軟骨細胞を、患者から採血した血液の血球以外の成分を使って培養し、最終的には細胞を数にして約1000倍にまで増やし、その細胞を、アテロコラーゲンハイドロゲルとポリ乳酸多孔体によって構成される再生医療用の特殊な素材(足場素材)に投与することで再生軟骨を作る。患者の軟骨は耳の裏から少量採取するだけなので、手術の傷は目立たず、耳の変形もほとんど残らないという。
インプラント型再生軟骨の製造方法
また、同再生軟骨は、注入するのではなく、「手術で埋め込む」ことができるという意味から「インプラント」型再生軟骨と名付けられた。今回開発された同再生軟骨の大きさは、長さ約50mm、幅約6mm、厚さ約3mmとなっている。
インプラント型再生軟骨の使用方法
すでに同型再生軟骨を鼻の高度な変形を患う口唇口蓋裂の患者に用いた臨床研究は東京大学医学部附属病院顎口腔外科・歯科矯正歯科の高戸毅教授、ティッシュ・エンジニアリング部星和人特任准教授(軟骨・骨再生医療寄付講座)らによって始まっている。口唇口蓋裂は先天性異常の1つで、生まれつき唇の一部や上あごが裂けている病気。鼻は顔の中心部に位置するため、鼻の変形の修正は患者にとって重要な治療だが、これまでは、鼻の高度な変形を治せるような大きな軟骨を身体から採取することができなかった。しかし、同再生軟骨を用いて治療することで、目立たない部位からわずかな軟骨を採取するだけで高度な変形が治療できるようになることが期待されるという。
インプラント型再生軟骨の概要
なお、NEDOでは、この臨床研究に続き、臨床試験(治験)を実施して産業化を展開していく計画とするほか、同技術を応用したNEDOプロジェクト「次世代機能代替技術の研究開発」により、細胞培養期間のさらなる短縮化、培養工程の簡素化を実現する再生デバイスの開発を行っていくとしている。
ピルクス、シリアルサーボをPCから制御できるUSBアダプタ製品を発売

ホビーロボットなどで使用できるシリアル通信式サーボモータ(シリアルサーボ)などを開発しているピルクスは、ホビーロボット向けUSBアダプタ「Pirkus USB シリアル通信アダプタ」(型番:PRS-SR001)など3点の発売を開始した。
Pirkus USB シリアル通信アダプタ(画像1)は、PCから直接同社のシリアルサーボの設定したり、操作したりするための橋渡しを行う周辺機器。設定や操作は、同社が配布しているシリアルサーボ専用ソフトを利用すすることで容易に行えるようになる仕組みだ。
スペックは、ボーレートが4800bps~1.25Mbps、通信レベルがTTL、USBコネクタの特機を除いた本体サイズは53mm×20mm×8mmとなっている。価格は5880円。
そして、Pirkus USB シリアル通信アダプタに「シリアルサーボHUB」(型番:PHB-002)と30cmのシリアルサーボHUB接続用ケーブル(型番:PRS-SR001-CB)の2点を加えたセットが、「Pirkus USB シリアル通信アダプタ シリアルサーボHUBセット」だ(画像2)。こちらは、価格が6930円となっている。
最後は、上記のセット内に含まれているシリアルサーボHUB接続用ケーブル単品。こちらは1050円となっている。
画像1。Pirkus USB シリアル通信アダプタ。USBメモリのような形状。USBコネクタと反対側にケーブルを接続する
画像2。Pirkus USB シリアル通信アダプタ シリアルサーボHUBセット。Pirkus USB シリアル通信アダプタ、シリアルサーボHUB、シリアルサーボHUB接続用ケーブルの3点セット。ケーブルは単体でも販売されている
Intersil、デュアルチャネル高速6A MOSFETドライバを発売

Intersilは9月6日(米国時間)、デュアルチャネル構成でともに最大6Aのドライブ能力を備えたMOSFETドライバ「ISL89367」を発表した。
同製品は、伝搬遅延25nsならびに20nsの立ち上がり/立ち下がりゲート信号でMOSFETをドライブするため、4.5Vから16Vを入力電圧範囲とする他のデバイスに比べてMOSFETで発生する電力損失を少なくすることが可能だ。
また、ハイサイドMOSFETおよびローサイドMOSFETの同時オンによる貫通電流を防止できるほか、効率の向上、EMIの抑制のために、ゲート信号のスイッチング遅延時間がプログラムできるようになっている。
ゲート信号のプログラム可能な遅延時間は内蔵タイマーによって最大270nsとなっているが、より大きな遅延が必要なアプリケーションにも対応できるように、高精度の入力スレッショルド性能を持つコンパレータを内蔵しており、これにより、簡単なRC回路によって、さらに大きな遅延を持たせることも可能となっているほか、高精度な入力スレッショルドにより、絶縁型電源アプリケーションで、2次トランス側の同期整流回路の設計を簡素化することが可能になると同社では説明している。
なお、同製品は4mm×4mmサイズの16ピンTDFNパッケージで、すでに量産受注を開始しており、1,000個受注時の単価は4.00ドルとしている。
デュアルチャネル6A MOSFETドライバ「ISL89367」
